Ngày nay, tế bào gốc đang là một chủ để rất “nóng” cả trong nghiên cứu và trị liệu bệnh mặc dù đây là lĩnh vực mới chỉ phát triển mạnh mẽ trong hơn một thập kỉ trở lại đây. Nhưng sự tiến bộ của khoa học và công nghệ đã giúp khai thác tiềm năng to lớn của tế bào gốc, đặc biệt là ứng dụng trong y học tái tạo hay điều trị bệnh. Tuy nhiên, thực tế cho thấy sự “thổi phồng” của truyền thông về tiềm năng ứng dụng của tế bào gốc trong xã hội có thể dẫn tới những hiểu lầm cho người dân và là cơ hội trục lợi của các công ty thương mại hoạt động trong lĩnh vực này. Nguy hiểm hơn đó là xuất hiện những trường hợp nghiên cứu và sử dụng tế bào gốc vi phạm luật pháp, đạo đức dẫn tới những hậu quả nghiêm trọng về tính mạng và của cải cho bệnh nhân.

Trong bối cảnh mà thế giới nói chung và Việt Nam nói riêng chưa có các quy định, các nguyên tắc đạo đức, các hướng dẫn cụ thể về nghiên cứu và sử dụng tế bào gốc thì việc cung cấp những thông tin chính xác, khoa học về tế bào gốc cho truyền thông, xã hội sẽ giúp người dân hiểu đúng về lĩnh vực mới, tiềm năng nhưng cũng không ít rủi ro này. Trong loạt bài này, chúng tôi xin được cung cấp các thông tin cơ bản về tế bào gốc, những thông tin này được trích dẫn từ Hiệp Hội Quốc Tế Về Nghiên Cứu Tế Bào Gốc (International Society For Stem Cell Research – ISSCR), do đó có thể đảm bảo một nguồn tin chính thống và khoa học về tế bào gốc. ISSCR là một tổ chức độc lập phi lợi nhuận và là tiếng nói chung của cộng đồng tế bào gốc. ISSCR được thành lập từ năm 2002 để thúc đẩy việc trao đổi thông tin về tế bào gốc và hiện nay có trên 4,100 thành viên khắp thế giới.
HIỂU ĐÚNG VỀ TẾ BÀO GỐC
1. Tế bào gốc là gì?
Tế bào gốc – Stem cell là những tế bào hình thành nên cơ thể. Các tế bào chuyên hóa của cơ thể ở các mô hay cơ quan khác nhau (ví dụ như tế bào gan ở gan, tế bào cơ ở cơ hay tế bào tim ở tim gọi là những những tế bào chuyên hóa chức năng hay những tế bào đã biệt hóa) đều có nguồn gốc từ những tế bào gốc ban đầu, những tế bào gốc ban đầu này hình thành không lâu sau quá trình thụ tinh của giao tử. Cơ thể của chúng ta duy trì trong suốt đời là nhờ vào sự tồn tại của các tế bào gốc ở các mô hằng ngày vẫn sửa chữa các tổn thương và thay thế các tế bào bị mất đi mỗi ngày ở các mô như da, tóc, máu hay ở đường tiêu hóa.
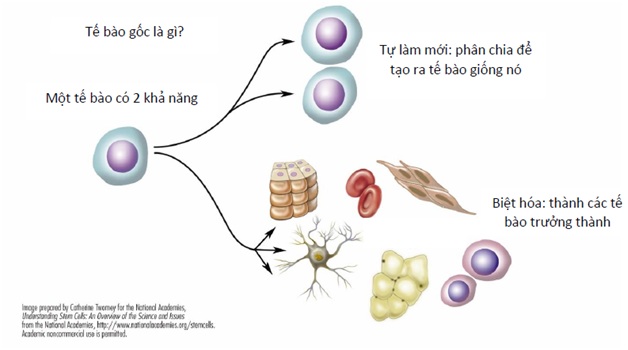
Tế bào gốc thường được xác định bởi hai đặc tính hay còn gọi là “đặc tính cơ bản của tế bào gốc”: khả năng tự làm mới – self renew (tức là khả năng phân chia để tạo ra các tế bào gốc khác) và khả năng biệt hóa – differentiate (tức là khả năng trở thành những tế bào trưởng thành, chuyên hóa chức năng trong các mô và cơ quan). Như vậy, hoàn toàn có thể nói một tế bào là tế bào gốc khi nó có cả hai đặc tính trên.
2. Các loại tế bào gốc
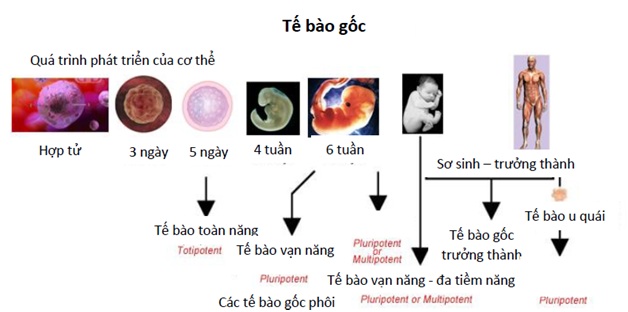
Dựa vào vị trí hay giai đoạn thu nhận tế bào gốc trong cơ thể. Có thể chia tế bào gốc thành các loại tế bào gốc chính như sau. Tế bào gốc phôi – embryonic stem cell là những tế bào tồn tại trong giai đoạn sớm của quá trình phát triển, tế bào gốc ở mô hay tế bào gốc trưởng thành – “tissue – specific” hay “adult” stem cell tồn tại trong suốt quá trình phát triển thai và trong suốt đời sống của cơ thể. Ngoài ra, gần đây các nhà khoa học tạo ra được một loại tế bào gốc nhân tạo gọi là tế bào gốc vạn năng cảm ứng – induced pluripotent stem cell hay iPS cell. Đây là những tế bào gốc không tìm thấy trong cơ thể nhưng lại được tạo ra bằng công nghệ từ những tế bào chuyên hóa trong cơ thể như da, iPS có đặc tính giống như tế bào gốc phôi. Từ các loại tế bào gốc chính ở trên, có thể chia ra nhiều nhóm tế bào gốc khác nhau trong đó với tên gọi dựa trên nguồn gốc phát triển phôi (tế bào gốc nội mô, trung mô) hay tiềm năng biệt hóa thành bao nhiêu loại tế bào trong cơ thể (tế bào toàn năng – hợp tử, tế bào vạn năng – tế bào gốc của phôi có thể phát triển thành tất cả các mô của cơ thể…, tế bào đa tiềm năng – tế bào gốc trưởng thành có thể phát triển thành nhiều hơn hai loại tế bào, hay tế bào đơn tiềm năng chỉ phát triển thành một loại tế bào…).
3. Tế bào gốc trưởng thành là gì? Nguồn gốc của chúng?
Tế bào gốc trưởng thành hay tế bào gốc ở mô là những tế bào đa tiềm năng – multipotent, có nghĩa là chúng có thể phát triển thành một số lượng giới hạn các loại tế bào trưởng thành, thường là các tế bào ở mô mà nó cư ngụ. Một số tế bào gốc ở mô chỉ có thể phát triển thành một hoặc hai loại tế bào trưởng thành. Các tế bào này gọi là các tế bào hai tiềm năng – bipotent và đơn tiềm năng – unipotent. Tế bào gốc trưởng thành được cho là có tiềm năng hình thành các loại tế bào của nhiều mô khác nhau chứ không chỉ là các loại tế bào từ mô nó cư ngụ, tuy nhiên, vấn đề này vẫn còn nhiều tranh cãi trong cộng đồng khoa học.
Nhiều mô chứa các tế bào gốc có thể thay thế các tế bào chết và khôi phục mô sau tổn thương. Da, cơ, ruột non và tủy xương là những mô điển hình, ở đó có chứa những tế bào gốc tại mô. Trong tủy xương, hàng tỷ tế bào máu mới được tạo ra mỗi này từ những tế bào gốc tạo máu. Hiện nay, vẫn chưa rõ có phải mọi cơ quan ở người trưởng thành đều có tế bào gốc hay không.
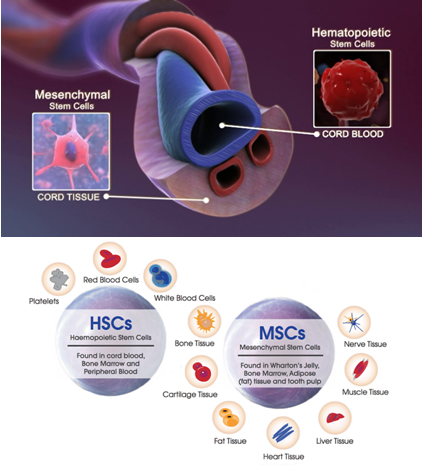
Các tế bào gốc ở mô thường hiếm, khó phân lập và nuôi cấy. Tế bào gốc tạo máu – hematopoietic stem cell hay blood forming stem cell – là loại tế bào được nghiên cứu nhiều nhất, nó tồn tại trong tủy xương, liên tục tạo để thay thế các tế bào máu. Hơn nữa, tủy xương còn chứa tế bào gốc trung mô – mesenchymal stem cell, có thể phát triển thành các tế bào sụn, mỡ và xương.
4. Tế bào gốc phôi là gì? Nguồn gốc thu nhận? Lợi ích của việc nghiên cứu tế bào gốc phôi?
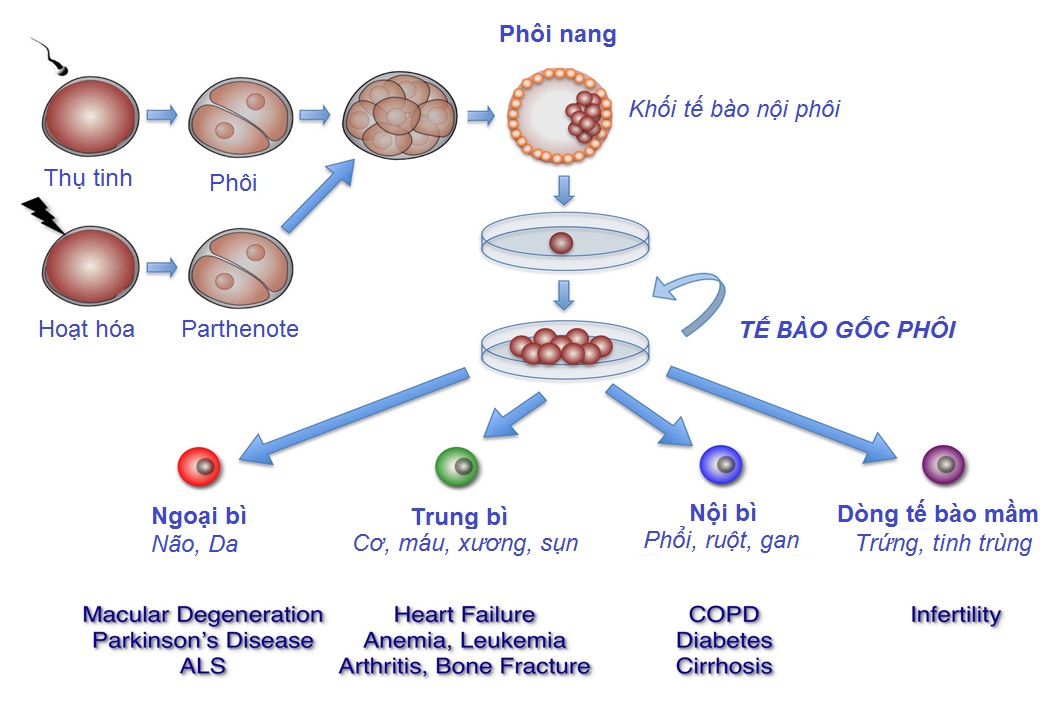
Tế bào gốc phôi – Embryonic stem cell –ESC là những tế bào gốc vạn năng – pluripotent, có nghĩa là chúng có thể phát triển thành tất cả các loại tế bào trong cơ thể. Trong phòng thí nghiệm (in vitro) các tế bào này có thể phát triển không giới hạn khi gặp điều kiện nuôi cấy tối ưu, và có thể biệt hóa thành nhiều loại tế bào trưởng thành, chuyên hóa chức năng khác nhau khi bổ sung các tín hiệu biệt hóa phù hợp vào môi trường nuôi cấy. Chính vì vậy mà chúng có giá trị rất lớn trong y học tái tạo (regenerative medicine). Các nghiên cứu hiện nay tập trung tìm cách tạo ra tế bào hoặc mô từ ESC để thử thuốc hoặc thay thế các cơ quan tổn thương cho người bệnh.
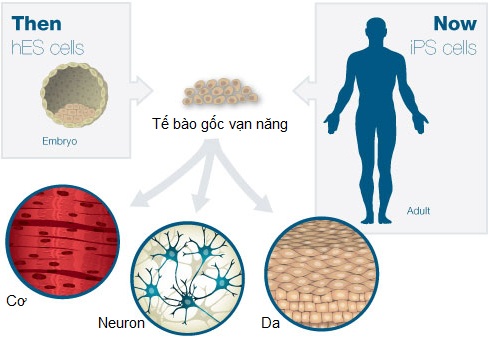
ESC có thể thu nhận từ giai đoạn sớm trong quá trình phát triển phôi, thông thường ở giai đoạn phôi nang (blastocyte), sau khoảng 5 ngày thụ tinh ở người. Phôi nang có hình dạng như một quả bóng rỗng không nhìn thấy được bằng mắt thường. Bên trong nó chứa một cụm khoảng 150 tế bào, cụm tế bào này gọi là khối nội phôi bào (inner cell mass – ICM), đây là những tế bào sẽ phát triển thành toàn bộ cơ thể. ESC là những tế bào ICM được thu nhận và nuôi cấy trong phòng thí nghiệm.
ESC của chuột lần đầu tiên được phân lập là vào năm 1981 và đang được sử dụng rộng rãi nhất trong nghiên cứu cho tới nay. Nghiên cứu ESC đã cho chúng ta biết rất nhiều về cách mà tế bào vạn năng tăng trưởng và chuyên hóa, về cách phát triển trong giai đoạn sớm diễn ra như thế nào. ESC của chuột có thể được thao tác làm thay đổi di truyền của một số gen cụ thể và để tạo ra chuột biến đổi gen đó, qua đó, khám phá ra rất nhiều bệnh liên quan tới di truyền ở người và giúp chúng ta hiểu về sự hình thành và phát triển của bệnh. Phương pháp này đã mang về giải Nobel trong lĩnh vực Sinh Lý Học và Y Học năm 2007 cho ba nhà phát minh là Capecchi, Evans và Smithies.
ESC của người mới được phân lập gần đây là vào năm 1998. ESC của người gặp nhiều khó khăn trong thao tác hơn so với của chuột, và hiện nay có rất ít hiểu biết về chúng. Tuy nhiên, nhờ đó mà các nhà khoa học đạt được những bước tiến lớn trong tìm hiểu sự phát triển của người, mô hình phát triển bệnh và chiến lược phát triển các liệu pháp mới trong điều trị bệnh.
5. Tế bào gốc “vạn năng cảm ứng” hay iPS cell là gì?
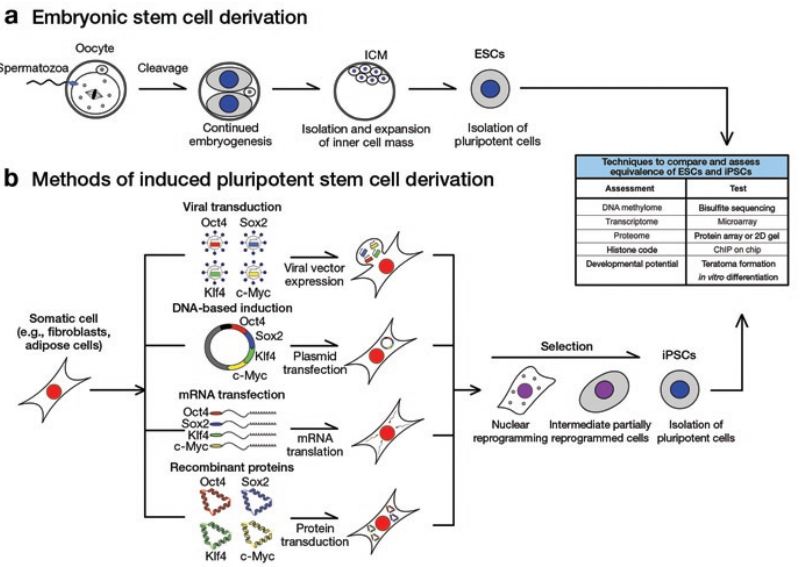
Tế bào iPS là những tế bào không còn tiềm năng biệt hóa (non-pluripotent) được cảm ứng để trở nên vạn năng, có nghĩa là có khả năng tạo ra tất cả các tế bào của cơ thể. Nói cách khác, đây là một tế bào đã chuyên hóa chức năng (như tế bào da) được “tái thiết lập chương trình – reprogrammed” để trở lại trạng thái “chưa chuyên hóa – unspecialized” tương tự như ESC. Tuy nhiên, iPS và ESC có nhiều đặc điểm không tương đồng.
Tế bào iPS chuột được tạo ra thành công năm 2006 và tế bào iPS người là vào cuối năm 2007.
Tế bào iPS được tạo ra bằng cách gắn chèn ba đến bốn gen giữ vai trò quan trọng trong ESC bằng virus vào các tế bào trưởng thành, như tế bào da hay tế bào miễn dịch. Các nhóm nghiên cứu khác nhau sử dụng các tổ hợp gen khác nhau và bằng các phương pháp khác nhau để chuyển gen vào trong tế bào. Hiện nay các nhà khoa học vẫn chưa hiểu hết chức năng của mỗi gen khác nhau góp phần vào tính vạn năng và cần các nghiên cứu xa hơn để trả lời cho câu hỏi này.
Tế bào iPS hứa hẹn sẽ tạo ra các dòng tế bào mô hình bệnh cho mục đích nghiên cứu. Tuy nhiên, vẫn cần nhiều nghiên cứu để có thể áp dụng phương pháp tạo tế bào này cho liệu pháp điều trị một cách an toàn và hiệu quả.
6. Liệu tế bào iPS có thể thay thế ESC trong nghiên cứu?
Tại thời điểm này, iPS không thể thay thế được ESC trong nghiên cứu. Mặc dù, iPS từ người mở ra nhiều hướng nghiên cứu mới hấp dẫn trong nghiên cứu tế bào gốc, công nghệ này đang ở những giai đoạn đầu và còn rất nhiều câu hỏi cơ bản cần được giải đáp. Trong khi iPS và ESC có nhiều đặc tính không tương đồng. Thì sự giống và khác giữa hai tế bào vẫn cần được nghiên cứu. Hơn thế nữa, để tạo ra iPS thì cần phải thao tác trên gen. Tác động lâu dài của việc thao tác và đặc biệt là khi cấy ghép trên bệnh nhân vẫn chưa biết. Với những lý do đó, ESC và iPS đều cần thiết trong nghiên cứu.
7. Tế bào gốc ung thư – cancer stem cell là gì?
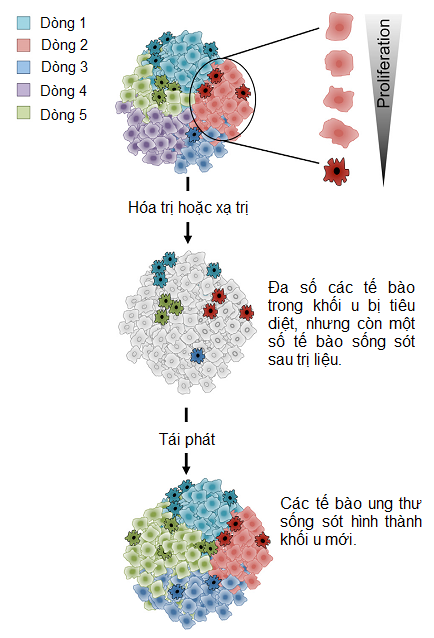
Tế bào gốc ung thư hay còn được dịch là tế bào ung thư có tính gốc – cancer stem cell – CSC là một quẩn thể phụ – subpopulation của các tế bào ung thư – cancer cell, nó có khả năng tự làm mới mạnh hơn các tế bào khác trong khối u và có khả năng hình thành khối u có đặc tính tương tự như khối u ban đầu khi cấy ghép những tế bào này lên chuột bị suy giảm miễn dịch. CSC được cho là những tế bào chịu trách nhiệm về sự phát triển và tái phát của khối sau trị liệu. Ở người, CSC có ở các loại ung thư khác nhau. Tuy nhiên, ở một số bệnh ung thư tiến triển, tỉ lệ các tế bào có đặc tính của tế bào gốc ung thư có thể rất cao. Hiện nay vẫn chưa hiểu tại sao các tế bào ung thư lại chứa các CSC, sự đóng góp của CSC vào sự phát triển của khối u là gì, vì sao CSC có thể kháng với các liệu pháp hóa hay xạ trị và cách tế bào gốc ung thư làm cho ung thư tái phát?
8. Dòng tế bào gốc – stem cell line là gì?
Dòng tế bào gốc – stem cell line là một quần thể tế bào có thể tự phân chia trong thời gian dài khi nuôi cấy in vitro (tức ở ngoài cơ thể). Các dòng tế bào phát triển khi được nuôi với điều kiện môi trường chứa các yếu tố tăng trường chuyên biệt, cùng với điều kiện về nhiệt độ và oxi, CO2 tương tự như trong cơ thể.

9. Tế bào gốc phôi có những tiềm năng ứng dụng gì?
A. Hiểu về sự phát triển của con người.
Hầu hết kiến thức về sự phát triển của người có được thông quan nghiên cứu các mô hình nghiên cứu như ruồi giấm, giun tròn, ếch và chuột. Dòng tế bào gốc phôi người có thể được nuôi cấy và biệt hóa thành các loại tế bào và mô khác nhau song song với những sự kiện sớm nhất của sự phát triển phôi, cho ta một cánh cửa duy nhất để tìm hiểu sự phát triển của người.
B. Nghiên cứu về các bệnh và sự hình thành các bệnh.
Các mô hình động vật thực nghiệm thường được sử dụng để nghiên cứu về bệnh của người trong phòng thí nghiệm, Tuy nhiên, nó không phải là mô hình chính xác cho những bệnh xuất hiện trên người. Tế bào gốc vạn năng của người, đặc biệt là của bệnh nhân hay những dòng tế bào mang bệnh cụ thể cho ta một mô hình bệnh của người chính xác hơn trong điều kiện phòng thí nghiệm.
C. Y học tái tạo
Thay thế các tế bào bị bệnh bằng cách tế bào khỏe mạnh, cách tiếp cận này gọi là y học tái tạo, đây là một ứng dụng đầy hứa hẹn của tế bào gốc. Ngày nay, các nhà nghiên cứu tìm cách sử dụng các tế bào gốc trưởng thành, tế bào gốc thai nhi và tế bào gốc phôi như là một nguồn cung cấp các loại tế bào khác nhau như tế bào thần kinh, tế bào cơ, tế bào máu và tế bào da để sử dụng trọng điều trị các bệnh khác nhau. Theo lý thuyết (chúng tôi nhấn mạnh là trong lý thuyết nó hoàn toàn có thể và thực tế người ta đang nỗ lực để hiện thực hóa nó), mọi trường hợp bệnh liên quan tới sự thoái hóa mô có thể được điều trị bằng liệu pháp tế bào gốc như bệnh liệt run (Parkinson), tổn thương dây cột sống, các bệnh tim, bệnh đái tháo đường type-1, loạn dưỡng cơ, thoái hóa thể vàng và bệnh gan. Tuy nhiên,một số trường hợp quan trọng cần xem xét khi hệ miễn dịch phá hủy các tế bào và gây ra bệnh như trong trường hợp bệnh đái tháo đường type 1 thì tế bào gốc biệt hóa thành các tế bào sản xuất insulin cũng có thể bị tấn công bởi hệ miễn dịch tương tự.
Thêm vào đó, một số loại tế bào gốc có di cư tới khối u hay vị trí tổn thương để tiết các yếu tố khác nhau để tác động lên sự đáp ứng của các tế bào khác như hệ miễn dịch tác động.
Các hướng tiếp cận này trong tương lai có thể thay đổi để phát triển các liệu pháp trị liệu dựa trên tế bào gốc.
10. Tại sao máu dây rốn – umbilical cord blood là một nguồn có giá trị?
Máu dây rốn – umbilical cord blood là nguồn giàu tế bào gốc tạo máu, hiện nay đang được thay thế cho cấy ghép tủy. Máu dây rốn có thể được thu nhận mà không gây xâm lấn từ dây rốn và bánh nhau sau sinh, sau đó kiểm tra, trữ lạnh trong ngân hàng mô để sử dụng khi cần. Yêu cầu về phù hợp người cho trong cấy ghép tế bào từ máu dây rốn ít nghiêm ngặt hơn các tế bào thông thường nên nhiều bệnh nhân có thể sử dụng mẫu tế bào máu dây rốn. Tuy nhiên, có thể do một mẫu máu dây rốn không có đủ số lượng tế bào gốc để điều trị cho người trưởng thành nên tế bào gốc máu dây rốn thường được sử dụng để điều trị cho trẻ em. Do đó, cần những nghiên cứu phát triển phương pháp nuôi cấy tăng sinh số lượng tế bào gốc trưởng thành ngoài cơ thể.
11. Tại sao các nhà nghiên cứu tập trung vào phát triển các tế bào gốc vạn năng ở các loại bệnh?
Sự phát triển các tế bào gốc vạn năng ở các loại bệnh có tiềm năng to lớn trong trị liệu vì hai nguyên nhân. Thứ nhất, các tế bào này cung cấp một công cụ hữu ích cho nghiên cứu nền tảng về bệnh ở người và để phát triển các loại thuốc mới. Thứ hai, các tế bào vạn năng ở các bệnh có thể phát triển thành loại tế bào cần để điều trị cho bệnh nhân đó. Khi cấy ghép lên chính người cho, các tế bào này sẽ được nhận diện như “bản thân”, vì vậy tránh vấn đề về thải loại và ức chế miễn dịch xuất hiện trong cấy ghép, cho dù người cho và người nhận có quan hệ tương đồng.
13. Chuyển nhân tế bào sinh dưỡng là gì?
Chuyển nhân tế bào sinh dưỡng – somatic cell nuclear transfer (SCNT) là một kỹ thuật trong đó nhân của tế bào sinh dưỡng (tế bào sinh dưỡng là mọi loại tế bào của cơ thể trừ các dòng tế bào sinh dục tinh trùng và trứng), được chuyển vào trứng đã loại bỏ nhân. Lúc này, trứng có DNA hay vật chất di truyền của tế bào sinh dưỡng cho nhân. Khi nhận được những tín hiệu phù hợp, trứng này có thể phát triển như là trứng được thụ tinh. Trứng được chuyển nhân sẽ phân chia hình thành 2 tế bào, sau đó là 4 tế bào, 8 tế bào và tiếp tục cho tới khoảng 150 tế bào ở giai đoạn phôi nang. Tế bào gốc phôi có thể thu nhận được từ giai đoạn phôi nang này để tạo ra những dòng tế bào có đặc tính di truyền tương tự như tế bào sinh dưỡng cho nhân.
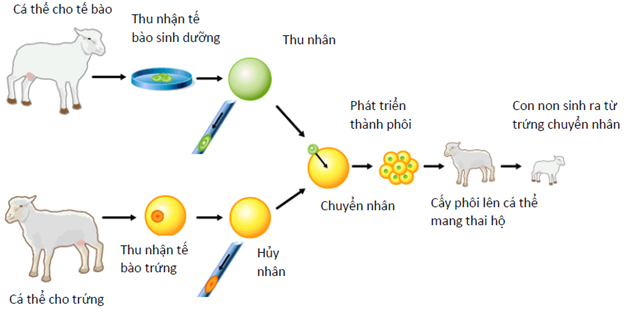
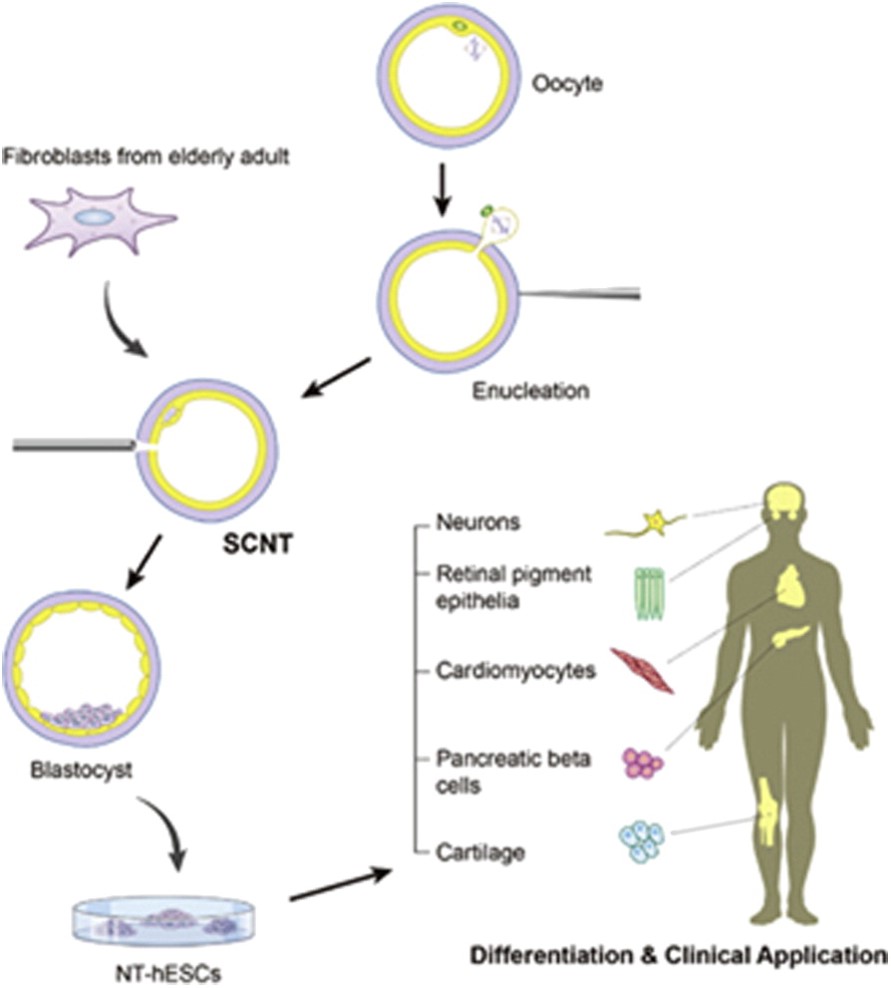
13. Tại sao lại sử dụng các dòng tế bào gốc phôi được thu nhận từ việc chuyển nhân tế bào sinh dưỡng (SCNT)?
Thứ nhất, các tế bào này là công cụ mới hữu ích để nghiên cứu đặc tính cơ bản của các bệnh ở người và để khám phá ra các loại thuốc mới. Thứ hai, các tế bào gốc phôi có thể phát triển thành các loại tế bào trưởng thành. Sau khi cấy ghép lên cơ thể cho nhân ban đầu, tế bào cấy ghép sẽ được nhận diện như là “bản thân” vì vậy mà tránh được các vấn đề về thải loại và ức chế miễn dịch gặp phải khi tế bào hoặc cơ quan cấy ghép được lấy từ người cho không tương thích. Điều này là hoàn toàn có thể tuy nhiên hiện này sự phát triển của tế bào iPS sẽ thay thế việc sử dụng chuyển nhân sinh dưỡng vì nó là kỹ thuật đơn giản hơn và không cần sử dụng tới tế bào trứng, tránh được các vấn đề về y đức khi thao tác trên trứng.
14. Y học tái tạo – regenerative medicine là gì?
Mục tiêu của y học tái tạo là sửa chữa cơ quan hay mô bị tổn thương do bệnh, lão hóa hay chấn thương, làm cho chức năng của nó được phục hồi hay cải thiện.
Thuật ngữ y học tái tạo – regenerative medicine được dùng hiện nay thường để mô tả các liệu pháp y khoa và các nghiên cứu sử dụng tới tế bào gốc (cả tế bào gốc trưởng thành và tế bào gốc phôi) để khôi phục chức năng của cơ quan hoặc mô. Điều này có thể đạt được bằng nhiều cách khác nhau; đầu tiên, sử dụng tế bào gốc hay tế bào biệt hóa từ tế bào gốc trong phòng thí nghiệm; thứ hai sử dụng thuốc kích hoạt tế bào gốc có sẵn trong mô để cải thiện hiệu quả sửa chữa tổn thương ở đó.
15. Tại sao việc nghiên cứu tế bào gốc quan trọng?
Nghiên cứu tế bào gốc góp phần vào các hiểu biết cơ bản về sự phát triển và hình thành cơ quan, cách thức mà các mô duy trì trong suốt đời sống. Những kiến thức này cần thiết để cung cấp các hiểu biết về những gì sai sót liên quan tới bệnh và tổn thương, qua đó suy ra các điều kiện có thể cần cho việc điều trị. Một khía cạnh đáng quan tâm trong lĩnh vực này là nghiên cứu tế bào gốc phôi người, vì những tế bào này mở ra một cánh cửa đặc trưng về sinh học và sự phát triển của người, từ đó mở ra các hiểu biết mới về các bệnh ở người.
Nghiên cứu về tế bào gốc phôi, chuyển nhân tế bào sinh dưỡng, tế bào gốc vạn năng cảm ứng (iPS cell) và tế bào gốc trưởng thành hay tế bào gốc ở mô cần phải tiến hành song song. Tất cả đều nằm trong nỗ lực nghiên cứu nhằm mục đích mở rộng kiến thức về hoạt động chức năng của tế bào, những sai hỏng gây ra bệnh, và làm thế nào giai đoạn đầu của sự phát triển của con người xảy ra. Từ đó, tổng hợp lại để cuối cùng có các liệu pháp điều trị an toàn và hiệu quả.
16. Đạo đức sinh học – bioethics là gì?
Đạo đức sinh học là nghiên cứu về các vấn đề xã hội, đạo đức, đạo lý trong lĩnh vực nghiên cứu khoa học, trị liệu y khoa và khoa học sự sống nói chung. Cùng với sự tiến bộ công nghệ hiện đại và những hiểu biết mới trong khoa học và các bệnh thì các vấn đề về y đức cũng được đặt ra.
17. Những dấu chấm hỏi về đạo đức trong nghiên cứu tế bào gốc là gì?
Một trong những câu hỏi thường được đặt ra trong nghiên cứu tế bào gốc đó là việc sử dụng phôi người để lấy tế bào gốc phôi là có đạo đức hay không có đạo đức? Tuy nhiên, bên cạnh đó còn nhiều vấn đề về đạo đức trong việc nghiên cứu tế bào gốc. Ví dụ như, để tạo ra các tế bào gốc vạn năng cảm ứng và tế bào gốc phôi từ chuyển nhân tế bào sinh dưỡng, các vật liệu sinh học phải được thu nhận từ người cho. Nên, có rất nhiều câu hỏi đặt ra về vấn đề quyền lợi của người cho.
Hơn thế nữa, với mọi trường hợp các liệu pháp có tiềm năng trị liệu trong y khoa, cũng cần thảo luận kỹ về cách sử dụng phương pháp điều trị và thời điểm bắt đầu thử nghiệm điều trị trên người và nếu thử nghiệm thành công thì làm cách nào để nó có thể ứng dụng trong điều trị trong thực tế.
Tham khảo: http://www.isscr.org/visitor-types/public/stem-cell-faq
Theo Biomedia Việt Nam